1
Patel MR, Peterson ED, Dai D, Brennan JM, Redberg RF, Anderson HV, Brindis RG and Douglas PS. Low diagnostic yield of elective coronary angiography. N Engl J Med. 2010;362:886-95.
2
Douglas PS, Hoffmann U, Patel MR, Mark DB, Al-Khalidi HR, Cavanaugh B, Cole J, Dolor RJ, Fordyce CB, Huang M, Khan MA, Kosinski AS, Krucoff MW, Malhotra V, Picard MH, Udelson JE, Velazquez EJ, Yow E, Cooper LS, Lee KL and Investigators P. Outcomes of anatomical versus functional testing for coronary artery disease. N Engl J Med. 2015;372:1291-300.
3
Shaw LJ, Berman DS, Picard MH, Friedrich MG, Kwong RY, Stone GW, Senior R, Min JK, Hachamovitch R, Scherrer-Crosbie M, Mieres JH, Marwick TH, Phillips LM, Chaudhry FA, Pellikka PA, Slomka P, Arai AE, Iskandrian AE, Bateman TM, Heller GV, Miller TD, Nagel E, Goyal A, Borges-Neto S, Boden WE, Reynolds HR, Hochman JS, Maron DJ, Douglas PS, National Institutes of Health/National Heart L and Blood Institute-Sponsored ITI. Comparative definitions for moderate-severe ischemia in stress nuclear, echocardiography, and magnetic resonance imaging. JACC Cardiovascular imaging. 2014;7:593-604
4
Phillips LM, Hachamovitch R, Berman DS, Iskandrian AE, Min JK, Picard MH, Kwong RY, Friedrich MG, Scherrer-Crosbie M, Hayes SW, Sharir T, Gosselin G, Mazzanti M, Senior R, Beanlands R, Smanio P, Goyal A, Al-Mallah M, Reynolds H, Stone GW, Maron DJ and Shaw LJ. Lessons learned from MPI and physiologic testing in randomized trials of stable ischemic heart disease: COURAGE, BARI 2D, FAME, and ISCHEMIA. Journal of nuclear cardiology : official publication of the American Society of Nuclear Cardiology. 2013;20:969-75.
5
Kang SJ, Mintz GS, Pu J, Sum ST, Madden SP, Burke AP, Xu K, Goldstein JA, Stone GW, Muller JE, Virmani R and Maehara A. Combined IVUS and NIRS detection of fibroatheromas: histopathological validation in human coronary arteries. JACC Cardiovascular imaging. 2015;8:184-94.
6
Kini AS, Baber U, Kovacic JC, Limaye A, Ali ZA, Sweeny J, Maehara A, Mehran R, Dangas G, Mintz GS, Fuster V, Narula J, Sharma SK and Moreno PR. Changes in plaque lipid content after short-term intensive versus standard statin therapy: the YELLOW trial (reduction in yellow plaque by aggressive lipid-lowering therapy). Journal of the American College of Cardiology. 2013;62:21-9.
7
Puri R, Nissen SE, Shao M, Uno K, Kataoka Y, Kapadia SR, Tuzcu EM and Nicholls SJ. Impact of baseline lipoprotein and C-reactive protein levels on coronary atheroma regression following high-intensity statin therapy. The American journal of cardiology. 2014;114:1465-72.
8
Pu J, Mintz GS, Biro S, Lee JB, Sum ST, Madden SP, Burke AP, Zhang P, He B, Goldstein JA, Stone GW, Muller JE, Virmani R and Maehara A. Insights into echo-attenuated plaques, echolucent plaques, and plaques with spotty calcification: novel findings from comparisons among intravascular ultrasound, near-infrared spectroscopy, and pathological histology in 2,294 human coronary artery segments. Journal of the American College of Cardiology. 2014;63:2220-33.
9
Dohi T, Maehara A, Moreno PR, Baber U, Kovacic JC, Limaye AM, Ali ZA, Sweeny JM, Mehran R, Dangas GD, Xu K, Sharma SK, Mintz GS and Kini AS. The relationship among extent of lipid-rich plaque, lesion characteristics, and plaque progression/regression in patients with coronary artery disease: a serial near-infrared spectroscopy and intravascular ultrasound study. European heart journal cardiovascular Imaging. 2015;16:81-7.
10
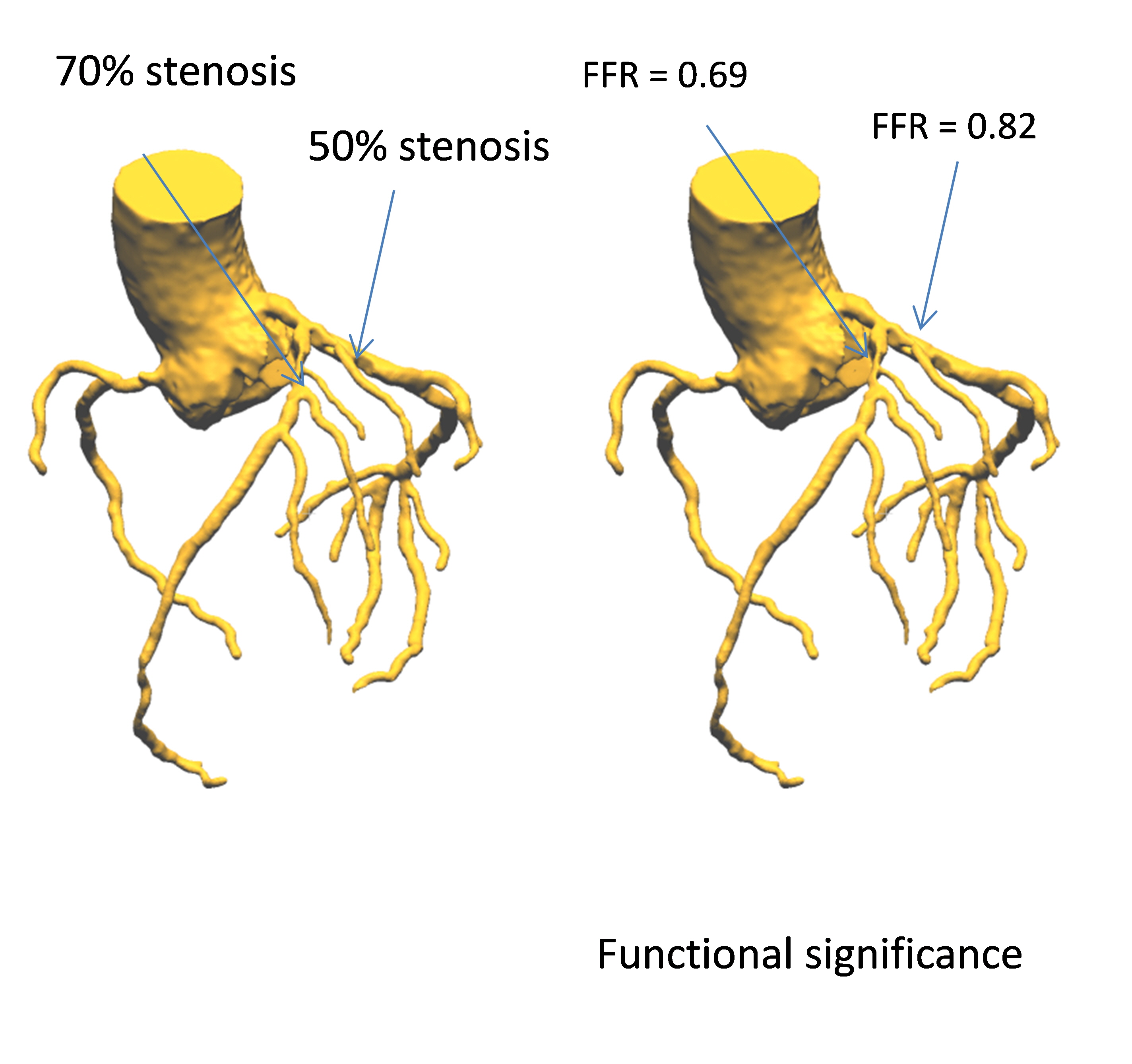
Coenen A, Lubbers MM, Kurata A, Kono A, Dedic A, Chelu RG, Dijkshoorn ML, Gijsen FJ, Ouhlous M, van Geuns RJ and Nieman K. Fractional flow reserve computed from noninvasive CT angiography data: diagnostic performance of an on-site clinician-operated computational fluid dynamics algorithm. Radiology. 2015;274:674-83.
11
Kwon SS, Chung EC, Park JS, Kim GT, Kim JW, Kim KH, Shin ES and Shim EB. A novel patient-specific model to compute coronary fractional flow reserve. Progress in biophysics and molecular biology. 2014;116:48-55.
12
Taylor CA, Fonte TA and Min JK. Computational fluid dynamics applied to cardiac computed tomography for noninvasive quantification of fractional flow reserve: scientific basis. Journal of the American College of Cardiology. 2013;61:2233-41.
13
Hong SJ, Kim BK, Shin DH, Kim JS, Hong MK, Gwon HC, Kim HS, Yu CW, Park HS, Chae IH, Rha SW, Lee SH, Kim MH, Hur SH, Jang Y and Registry KC. Usefulness of intravascular ultrasound guidance in percutaneous coronary intervention with second-generation drug-eluting stents for chronic total occlusions (from the Multicenter Korean-Chronic Total Occlusion Registry). The American journal of cardiology. 2014;114:534-40.
14
Nasis A, Mottram PM, Cameron JD and Seneviratne SK. Current and evolving clinical applications of multidetector cardiac CT in assessment of structural heart disease. Radiology. 2013;267:11-25.
15
Clemente A, Avogliero F, Berti S, Paradossi U, Jamagidze G, Rezzaghi M, Della Latta D and Chiappino D. Multimodality imaging in preoperative assessment of left atrial appendage transcatheter occlusion with the Amplatzer Cardiac Plug. European heart journal cardiovascular Imaging. 2015.
16
Romero J, Cao JJ, Garcia MJ and Taub CC. Cardiac imaging for assessment of left atrial appendage stasis and thrombosis. Nat Rev Cardiol. 2014;11:470-80.
17
Theriault-Lauzier P, Andalib A, Martucci G, Mylotte D, Cecere R, Lange R, Tchetche D, Modine T, van Mieghem N, Windecker S, Buithieu J and Piazza N. Fluoroscopic anatomy of left-sided heart structures for transcatheter interventions: insight from multislice computed tomography. JACC Cardiovascular interventions. 2014;7:947-57.
18
Kapadia SR, Schoenhagen P, Stewart W and Tuzcu EM. Imaging for transcatheter valve procedures. Current problems in cardiology. 2010;35:228-76.