 메뉴열기
메뉴열기
Based on B.L. Nørgaard, B. Ko. Angiography based quantitative flow ratio in coronary artery disease: Mimic of FFR – Ready for clinical use? Int J Cardiol. 2019 Mar 15;279:29-30
압력철선 (pressure wire) 을 이용한 분획 혈류 예비력 (fractional flow reserve, FFR) 검사법은 일반적으로 아데노신으로 유도되는 최대충혈 (hyperemia) 상태에서, 대동맥의 압력 대비 협착부위 원거리 지점의 압력의 비율로 정의된다. FAME 연구에서, 허혈증을 정의하기 위해 FFR 0.8 이하를 임계값으로 사용하여 중재시술 (percutaneous coronary intervention, PCI) 시행여부를 결정한 것이 혈관 조영 유도 PCI와 비교하였을 때 개선된 임상성적 결과를 가져왔다1. 그러나, FFR 검사는 관상동맥 내 침습적 시술 및 전신혈관의 확장을 유발하는 약제의 사용, 추가적인 시술 시간의 필요성, 이로 인한 환자의 불편감 및 합병증 등의 위험성이 있다. Instantaneous wave-free ratio (IFR) 과 resting Pd/Pa 비율 등의 안정시 지표들을 사용하면 최대충혈을 유도할 필요가 없고, 최근 발표된 2개의 다기관 연구에서 iFR을 통한 PCI 결정법이 FFR 이용법과 동등한 1년 임상결과를 입증하였다. 그렇지만 FFR과 마찬가지로 이 검사법들은 모두 침습적인 wire 를 관상동맥 내에 위치하여야 하는 한계가 있으며, 또한 그로 인한 비용적 부담 등을 이유로 보편화되지 못하고 있다. 2 따라서, 최근 다양한 혈류 시뮬레이션 전략을 통해 비침습적으로 관상동맥 내 압력변화를 예측하려는 기법들 (FFR CT 와 Quantitative flow ratio) 이 개발되었다.
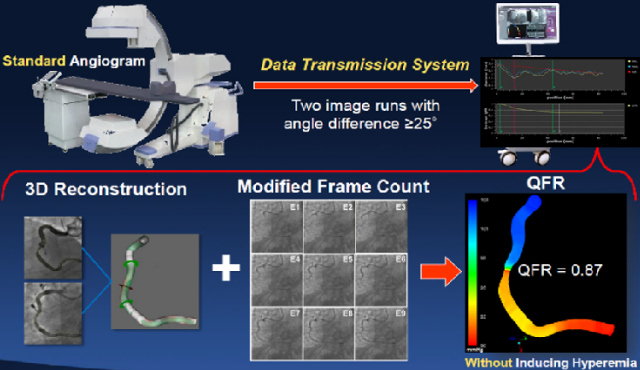
QFR (quantitative flow ratio)은 침습적인 와이어의 사용이 필요 없고, 최대충혈을 유발시키는 adenosine/nicorandil 등의 약제 사용이 필요 없는 방법으로 접근성과 안전성이 좋은 장점이 있다. 심혈관 조영술을 시행한 후 중등도 협착 병변이 있는 목표혈관에 대해 25도 이상의 각도 차이로 찍은 조영술 영상 2개를 바탕으로 혈관을 3D reconstruction 하여 CFD (computational fluid dynamics) 알고리즘으로 계산하여 협착부위 전후 압력감소 정도를 분석한 virtual FFR measurement 기법이다 (Fig. 1)3. 이 CFD 알고리즘은 조사된 TIMI frame count 를 바탕으로 얻어낸 혈류속도를 기반으로 최대 충혈시 혈류속도를 예측하는 근사 경험식과 마찰 및 유동박리로 인한 압력감소 관계 계산식을 포함한다. QFR은 기하학적 구조를 기반으로 하고, 복잡한 CFD 분석이 아니기 때문에 몇 분 안에 계산할 수 있다. 중등도 협착 병변에 대한 QFR의 예후 예측력을 검증한 기존 연구들에서 계산시간은 대략 7분, 높은 실행 가능성, FFR에 대한 80~93%의 양호한 진단 정확도를 보였다4-7.
FAVOR II pilot 연구를 통해 조영제 기반 contrast flow QFR 값이 실제 최대충혈을 유발한adenosine QFR 값에 근사하다는 연구결과를 보여줬다4. FFR≤0.8 에 대한 Contrast QFR ≤0.8 의 정확도는 86% 였으며 이는 adenosine QFR ≤0.8 의 87% 과 유효한 차이가 없어 hyperemia 의 유도 없이 검사할 수 있다는 결과가 발표되었다. 이 결과들을 바탕으로 FAVOR II China 연구에서는 300명 환자의 CAG검사중 실시간으로 시행한 online QFR≤0.8 이 FFR≤0.8 에 대해 92.4% 의 정확도와 94.6% 민감도, 91.7%의 특이도, 85.5% 양성 예측도, 97.1% 음성 예측도로 매우 높은 신뢰도를 보이며 침습적인 FFR 검사를 대신하여 비침습적인 QFR 검사의 사용을 제시하였다 (Fig. 2A)5.
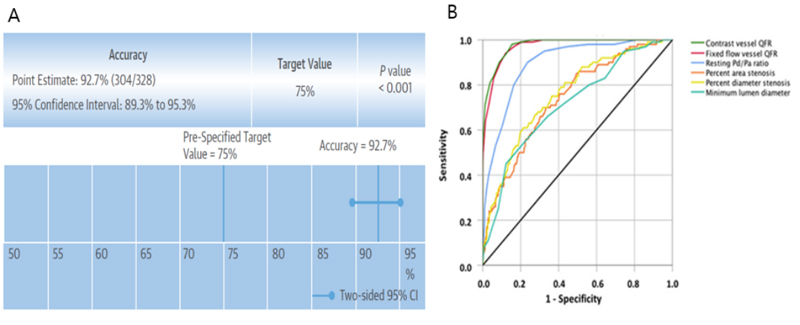
또한, 최근 436명 실제 임상 환자를 대상으로 한 연구에서 FFR≤0.8에 대한 조영제 기반 QFR≤0.8, resting Pd/Pa≤0.91, 최대 협착 직경 정도>50% (percent diameter stenosis)의 병변 특이 허혈 진단력을 비교 분석하였으며 AUC가 0.86, 0.76, 0.63 으로 확인되었다 (Fig. 2B)8. 90%의 혈관이 QFR으로 분석 가능하였으며, 조영제 기반 QFR≤0.8의 진단 정확도는 93.4%로 매우 높은 신뢰도를 보였다. 특히 QFR이 resting Pd/Pa ratio 보다 더 높은 진단력을 보인 점을 주목할 만 한데, 기존 연구들에서 resting Pd/Pa가 iFR 과 필적하게 해부학적 및 혈류역학 협착 심각도 그리고 임상결과 위험도와 연관성을 보여왔기 때문이다9. 그렇지만, 몇가지 고려해야 할 문제가 있다. 우선, 이 연구는 retrospective study 이며, 선택편견을 가질 수 있다. 더구나 3D-QCA 으로 평가되었을 때 <40% 의 협착을 보인 혈관이 40%나 포함이 되어있었다. 따라서, FFR≤0.8 으로 분석된 혈관 (19%)이 기존 연구들 (34%) 보다 적었으며 진단력을 높이는 결과를 가져왔을 수 있다. 진단 임계점 근처의 “gray zone” (0.75-0.85) 에 해당하는 전체의 40% 혈관 분석시 진단 정확도는 81%에 불과하였다. QFR은 아직 검증되어야 할 부분들이 많이 있다. Ostial, 분지 및 tandem 병변, 스텐트가 있는 혈관, 구불구불한 혈관, 심한 diffuse 병변, 그리고 미세혈관 기능장애, 부정맥이 있는 환자들에서는 어떻게 수행되는지 등이 이에 해당된다. 더욱이 gray zone에 해당된 병변에 대한 관찰자간 재현성 여부도 해결되어야 할 숙제일 것이다.
QFR의 초기 임상결과들은 침습적인 FFR 검사의 진단성능을 비교적 면밀히 모방하는 것으로 보고되었지만, 임상에 직접 적용하여 PCI여부를 결정하기 전에 보다 복잡한 관상동맥질환에서도 FFR을 대체할 수 있을지 더 많은 연구가 필요한 상황이다. 또한, 간과하면 안 되는 부분은, 이런 새로운 혈관 조영술 기반 FFR 분석법은 “lesion-specific”한 현재 상태의 정보를 제공해주는 것뿐이라는 점이다. FFR guided PCI 기법은 optimal medical therapy 와 비교하여 hard outcome의 개선으로 이어진다는 확실한 증거는 없는 실정이다. 현재와 미래의 심혈관 사고를 모두 잘 예방하기 위해서는 동맥경화반의 morphology 및 burden 같은 허혈 매개변수도 고려하여 약물치료를 조절하는 것이 필요하다. 추후 QFR에 기계학습 알고리즘을 추가하고, plaque vulnerability 기준지수를 기반으로 한 CFD 시뮬레이션 기법을 적용하면 보다 정교하고 유용한 분석법으로 발전할 수 있을 것이다.
1. Marcus ML, Skorton DJ, Johnson MR, Collins SM, Harrison DG, Kerber RE. Visual estimates of percent diameter coronary stenosis: "a battered gold standard". J Am Coll Cardiol 1988;11:882–885.
2. A.R. Ihdayhid, A. Yong, R. Harper, J. Rankin, C. Wong, A.J. Brown, et al., A practical guide for fractional flow reserve guided revascularisation, Heart Lung Circ. 27 (2018) 406–419.
3. Shengxian Tu, Emanuele Barbato, Zsolt Köszegi et al. Fractional Flow Reserve Calculation From 3-Dimensional Quantitative Coronary Angiography and TIMI Frame Count: A Fast Computer Model to Quantify the Functional Significance of Moderately Obstructed Coronary Arteries. J Am Coll Cardiovasc Intv 2014;7:768-77.
4. S. Tu, J.Westra, J. Yang, C. von Birgelen, A. Ferrara, M. Pellicano, et al., Diagnostic accuracy of fast computational approaches to derive fractional flow reserve fromdiagnostic coronary angiography: the international multicenter FAVOR pilot study, J. Am. Coll. Cardiol. Cardiovasc. Interv. 9 (2016) 2024–2035.
5. B. Xu, S. Tu, S. Qiao, et al., Diagnostic accuracy of angiography-based quantitative flow ratio measurements for online assessment of coronary stenosis, J. Am. Coll. Cardiol. 70 (2017) 3077–3087.
6. J. Westra, B.K. Andersen, G. Campo, H. Matsuo, L. Koltowski, A. Eftekhari, et al., Diagnostic performance of in-procedure angiography-derived quantitative flow reserve compared to pressure-derived fractional flow reserve: the FAVOR II Europe- Japan study, J. Am. Heart Assoc. 7 (2018), e009603.
7. J.Westra, S. Tu,Winther, et al., Evaluation of coronary artery stenosis by quantitative flow ratio during invasive coronary angiography. TheWIFI II study (Wire-free Functional Imaging II), Circ. Cardiovasc. Imaging e007107 (2018) 11.
8. B.E. Stähli, A. Erbay, J. Steiner, J. Klotsche, H.-C.Mochmann, C. Skurk, et al., Comparison of resting distal to aortic coronary pressure with angiography-based quantitative flow ratio, Int. J. Cardiol. 279 (2019) 12–17.
9. J.M. Lee, J. Park, D. Hwang, C.H. Kim, K.H. Choi, T.M. Rhee, et al., Similarity and differenceof resting distal to aortic coronary pressure and instantaneous wave-free ratio, J. Am. Coll. Cardiol. 70 (2017) 2114–2123